ЖИДКОСТИ

мент, когда сясатие Ж. сделается достаточно большим и молекулы могут оказывать друг на друга значительное воздействие, газ переходит в жидкое состояние. В веществе образуется поверхность раздела, отделяющая насыщенный пар от жидкости. При сжатии насыщенного пара его давление р остается постоянным, и пар переходит в Ж. (часть ВС). Наконец когда весь пар, находящийся под жидкостью, конденсируется и превращается в капельную Ж., под поршнем в приборе будет находиться исключительно капельная Ж., сжатие к-рой чрезвычайно мало и требует огромных давлений (часть CD). Если взять более высокую исходную t°, то пределы объемов, где наблюдают капельную Ж., будут меньше, напр. С1В1 для более высокой t°. Наконец можно нагреть Ж. до такой t°, когда жидкость будет только в одной точке образовывать насыщенные пары (точка К, на рис.). Это будет соответствовать критической t° (кривая MKN), переходя к-рую попадают в область газообразного состояния, характеризуемого для температур, далеких от критической, подчинением газа закону Бойля-Мариотта и Гей-Люссака (кривая PQ). (Область, где существует раздел между Ж. и паром, на рисунке очерчена пунктиром И Заштрихована.) П. Лазарев.
Частицы Ж., лежащие вблизи от ее поверхности (образующие поверхностный слой), втягиваются ниже лежащими молекулами внутрь Ж., тогда как находящиеся в глубине Ж. частицы притягиваются своими соседями одинаково во все стороны. Такие силы, действующие на поверхностные частицы Ж. перпендикулярно к ее поверхности и рассчитанные на 1 ел*2 ее, и дают молекулярное давление К = "j(no Ван-дер-Ваальсу). Отсюда ясно также, что для увеличения поверхности Ж. на 1 см2, т. е. для извлечения нек-рого числа частиц изнутри Ж. в ее поверхностный слой, надо затратить работу. Эта работа образования 1 см2 поверхности Ж. (<т), называемая поверхностным натяжением, измеряется в эрг/ам2=дин/ел( и накопляется в поверхностном слое в виде избытка свободной (т.н. «поверхностной») энергии его молекул a. s (s—поверхность) (сш.Поверхностное натяжение, Капилярность). Жидкая масса, предоставленная самой себе, всегда уменьшая свою свободную энергию в самопроизвольном процессе (при v и t° = const.), стремится к минимуму свободной энергии, т. е. к минимуму поверхности s, принимая форму шара. Шар при данном объеме обладает наименьшей поверхностью, и его надо рассматривать как естественную форму всех Ж. Так, малые капли Ж., форма которых мало искажается силой тяжести, шарообразны, если они напр. лежат на несмачиваемой пластинке (капли воды на парафине, ртути—на стекле). Малая сжимаемость Ж., /?=----• -.--, т. е. относительное уменьшение объема Ж. при приросте давления р на 1 atm [/? измеряется в обратных атмосферах (atm)"1], объясняется тем, что Ж. уже сжаты весьма большим молекулярным давлением (см. таблицу). Основные молекулярные свойства жидкостей (при t° = 20°). Жидкости Глицерин . . — Гликоль . . . — Этил, спирт . — Бензол .... 72,8 65,0 46,7 21,6 28,8 18.5 S5 46.МГ S В н° л о S о Ив 81,0 56,2 41,2 27,0 2,3 1,9 О-! ess 3,7 1,00 Для разных Ж. /J изменяется обратно молекулярному сцеплению, т. е. К и а (см. табл.); так, для ртути (<т=460 эрг/aw3) имеем весьма малую /?=3,9.10~в (atm)-"1. Все Ж. обычно ассоциированы в большей или меньшей степени, т. е. частицы их являются комплексами простых молекул. Так, жидкая вода состоит гл. обр. из «дигидроля» (Н20)2 и «тригидроля»(Н20)3. С повышением t° степень ассоциации Ж. обычно падает. Ассоциация Ж.обусловлена их полярностью, т. е. присутствием в их молекулах асимметрично расположенных полярныхгрупп,проявляющих вторичные валентности (ОН', NH/, СООН'). Молекулы полярных Ж. (вода, амины, спирты, органические кислоты) могут быть рассматриваемы как электрические диполи (см.): Междумолекулярные силы в полярных (ассоциированных) Ж. велики; они характеризуются большим поверхностным натяжением, внутренним давлением, скрытой теплотой испарения и диэлектрической постоянной (см. табл.). Неполярные Ж. (углеводороды) неассоциированы (т. н. нормальные Ж.) и обладают низкой диэлектрической постоянной, небольшим поверхностным натяжением и т. д. Чем больше различие в полярности двух соприкасающихся Ж., тем меньше их взаимная растворимость и тем больше поверхностное натяжение на границе между ними. С уменьшением разности в полярностях взаимная растворимость жидкостей растет, и жидкости, близкие по полярности, смешиваются друг с другом во всех отношениях (вода, спирт, ацетон). (См. также Капилярность, Поверхностное натяжение, Вязкость.} П. Ребиндер. Лит.: Б и р о н Е., Учение о газах и жидкостях, М.—П., 1923; Обреимов И., Состояние вещества, П., 1922; Хвольсон О., Курс физики, т. I, Берлин, 1923; Bakker G., Kapillaritat und Ober-flachenspannung (Hndb. der Experimentalphysik, hrsg. v. W. Wien u. F. Harms, B. VI, Leipzig, 1928); Freundlich H., Kapinarchemie, Lpz., 1922; J e 11 i n e k K., Lehrbuch der physikai. Cnemie, B. I, Stuttgart, 1928; Kreminn R., Mechanlsche Eigen-schafteii flussiger Stoffe, Leipzig, 1928.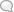 Смотрите также:
Смотрите также:
- ЖИЗНЕННАЯ ЕМКОСТЬ ЛЕГКИХ, максимальный объем воздуха, к-рый можно выдохнуть после максимального вдоха. У разных людей Ж. е. л. различна. В среднем у мужчин она равна 3.500—4.000 см3, у женщин 2.500—3.000 см3, но ...
- ЖИЗНЕННЫЕ ПРОБЫ,имеют существенное значение для разрешения вопроса о живорожденности плода при судебно-медицинских исследованиях трупов младенцев. Обычно как правило производятся легочная и желудочно - кишечная гидростатические пробы.Воснове легочной пробы(dokimasia pulmonalis) лежит факт ...
- ЖИЗНЕСПОСОБНОСТЬ, термин, обозначающий в судебной медицине способность плода к продолжению жизни вне утробы матери. Ж. обусловлена двумя моментами: достаточной зрелостью плода и отсутствием значительно выраженных пороков развития или б-ней. Невозможно ...
- ЖИЗНЬ. Содержание: Определение понятия «жизнь» ........292 Проблема возникновения жизни на земле . . 296 Жизнь с точки зрения диалектического материализма....................299 Жизнь, основное понятие, ...
- ЖИЛИЩЕ, может рассматриваться и изучаться во-первых как комплекс технически оформленных сан. условий в жизни человека в периоды его повседневного труда и отдыха в т. н. домашней обстановке и во-вторых как ...